近日,太阳成集团朱成建教授和谢劲教授团队报道了一种激发态镍-锂双金属协同的多氟芳烃与芳基氯的亲电交叉偶联新策略,实现了多氟芳烃中非常规C-F反应位点的高选择性芳基化。该策略不仅为含氟生物活性分子及功能材料的高效合成开辟了新方法,还有效改变了化学反应中的区域选择性,为其调控提供了重要参考。该研究论文以“Selective arylation of atypical C–F bonds in polyfluoroarenes with aryl chlorides”为题,于2025年10月3日发表在《Nature Chemistry》上。文章链接为:https://www.nature.com/articles/s41557-025-01962-1。
多氟芳烃和多氟杂芳烃在医药、农药和有机材料等领域具有广泛应用(图1a)。近几十年来,通过C-H或C-X键氟化一直是合成氟代芳环的重要方法。尽管这些方法能够高效合成多种单氟芳烃,但它们通常需要预先引入多个官能团或导向基团,因此将这些策略应用于多氟芳烃的合成中存在较大局限。利用廉价易得的多氟芳烃化工品为原料,通过直接脱氟官能团化策略已成为合成复杂多氟芳基化合物的有效方法。这些策略包括芳基亲核取代(SNAr)策略、光催化单电子还原(SET)策略以及金属催化C-F键活化策略等(图1b)。然而,大多依赖于有机锂、格氏试剂等金属亲核试剂的使用,或依赖光催化剂的氧化还原能力,这在一定程度上限制了其应用范围。
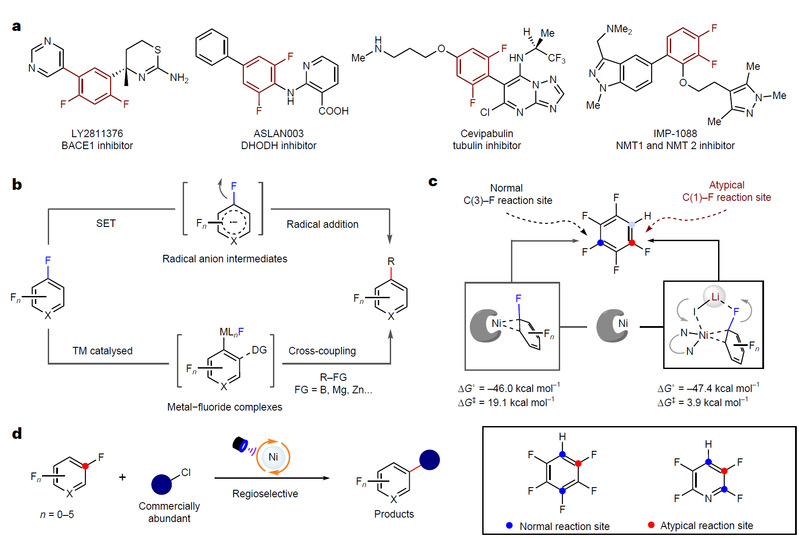
图1 多氟芳烃的官能团化。(图片来源:Nature Chemistry)
研究团队针对多氟芳烃选择性C-F键活化这一难题,另辟蹊径,提出一种锂-镍双金属协同策略。通过Li-F相互作用,他们成功实现了五氟苯C(1)-F位点的特异性活化,突破了传统Ni催化的C(3)-F位点反应的局限(图1c)。基于这一创新性活化模式,团队开发了一种多氟芳烃与氯代芳烃的C-F/C-Cl键亲电交叉偶联反应。该方法不仅展现了优异的位点选择性和底物兼容性,还为构建复杂含氟联芳烃提供了全新路径。
美国著名金属化学家Daniel J. Weix教授在Research Briefing中评论道:“Although cross-coupling of aryl fluorides with aryl nucleophiles has been reported, translating this to a cross-electrophile coupling with other aryl halides seemed impossible to me because of the exceptional stability of the C–F bond. I think this work is a notable advance for the field and a useful way to synthesize partially fluorinated biaryl compounds.”
该工作通讯单位为太阳集团tcy8722、配位化学国家重点实验室与化学与生物医药创新研究院(ChemBIC)。刘志博士为论文第一作者,太阳成集团谢劲教授、朱成建教授、李伟鹏助理教授以及韩杰副研究员为论文共同通讯作者。此项研究得到了国家重点研发计划(2022YFA1503200)、国家自然科学基金(22471121、22471122、22271144)、中央高校基本科研业务费(项目编号:020514380252)、化学和生物医药创新研究院、配位化学全国重点实验室和多靶标天然药物全国重点实验室的共同资助。
